從礦石或化合物中提煉金屬,是還原過程;而腐蝕則是將金屬氧化為礦石或化合物,是冶煉的逆過程,即氧化過程。這兩個過程的原理是可以相互借用的。干腐蝕為高溫氧化,濕腐蝕是電解液腐蝕。在液態或固態電解質中的金屬腐蝕過程是電化學過程,是一種涉及電子轉移的化學過程。因此,腐蝕能否進行,取決于金屬能否離子化;而金屬離子化的趨勢,可以用金屬的標準電極電位(ε)來表示。定性地講,金屬的標準電位越負,則越易離子化。
如,鋼表面(mian)生銹是電(dian)化學腐(fu)蝕(shi)的(de)結(jie)果。鋼暴(bao)露在大(da)氣(qi)中,表面(mian)吸附了一層很(hen)薄(bo)的(de)水(shui)膜,鋼表面(mian)不(bu)同的(de)電(dian)極(ji)電(dian)位和水(shui)膜構(gou)成了微電(dian)池(chi),就會引起電(dian)化學腐(fu)蝕(shi)。
鋼(gang)本身由于包含有碳(tan)化(hua)物(wu)(wu)、夾渣物(wu)(wu)等,各(ge)部(bu)分(fen)的(de)(de)組織和成分(fen)是不均(jun)勻(yun)的(de)(de),此外內部(bu)應力(li)也(ye)不均(jun)勻(yun),這些都促使各(ge)部(bu)分(fen)在電(dian)(dian)解質溶液中(zhong),產生(sheng)相互間的(de)(de)電(dian)(dian)極電(dian)(dian)位差。這種電(dian)(dian)極電(dian)(dian)位差愈(yu)(yu)大,微(wei)陽極和微(wei)陰極間的(de)(de)電(dian)(dian)流(liu)強度(du)愈(yu)(yu)大,鋼(gang)的(de)(de)腐蝕(shi)速(su)度(du)也(ye)愈(yu)(yu)大,結果(guo)是微(wei)陽極部(bu)分(fen)發(fa)生(sheng)嚴重的(de)(de)腐蝕(shi)。
這(zhe)種腐蝕(shi)微電(dian)池所引起電(dian)化學腐蝕(shi),在開(kai)始階段和腐蝕(shi)過程(cheng)中(zhong),就會產生陽極極化作(zuo)(zuo)用和陰(yin)極極化作(zuo)(zuo)用。
一、極化作用
在(zai)電化學腐蝕中,能(neng)夠控(kong)制腐蝕反應速(su)度(du)的(de)現象稱為極(ji)化,極(ji)化可使陽極(ji)與陰極(ji)參與反應的(de)速(su)度(du)得到減弱和減緩。
極(ji)(ji)化(hua)(hua)作用的(de)原(yuan)理 當電(dian)(dian)流通(tong)過原(yuan)來電(dian)(dian)池(chi)開始流動(dong)的(de)瞬(shun)間,在電(dian)(dian)極(ji)(ji)上產(chan)生化(hua)(hua)學變化(hua)(hua),這(zhe)些變化(hua)(hua)試圖(tu)建立一(yi)個新的(de)與(yu)原(yuan)來電(dian)(dian)池(chi)電(dian)(dian)壓(ya)(ya)方(fang)向(xiang)相反(fan)的(de)伏打(da)電(dian)(dian)池(chi)。這(zhe)種新的(de)反(fan)電(dian)(dian)壓(ya)(ya)稱為極(ji)(ji)化(hua)(hua),其方(fang)向(xiang)與(yu)原(yuan)來電(dian)(dian)池(chi)的(de)電(dian)(dian)壓(ya)(ya)方(fang)向(xiang)相反(fan),從而使(shi)原(yuan)來的(de)電(dian)(dian)池(chi)電(dian)(dian)壓(ya)(ya)得到了削弱(ruo)。也(ye)就是(shi)說(shuo),由于極(ji)(ji)化(hua)(hua)使(shi)得腐蝕電(dian)(dian)池(chi)中金屬的(de)各電(dian)(dian)位(wei)(wei)彼此相互接近 陽極(ji)(ji)電(dian)(dian)位(wei)(wei)的(de)下降
稱為(wei)陽(yang)極(ji)(ji)(ji)極(ji)(ji)(ji)化(hua)(hua)(hua),陰(yin)(yin)極(ji)(ji)(ji)電(dian)位的(de)(de)下降(jiang)(jiang)稱為(wei)陰(yin)(yin)極(ji)(ji)(ji)極(ji)(ji)(ji)化(hua)(hua)(hua)。電(dian)池電(dian)壓的(de)(de)下降(jiang)(jiang)、減(jian)小(xiao)使(shi)得流過(guo)電(dian)池的(de)(de)電(dian)流也減(jian)小(xiao)。陽(yang)極(ji)(ji)(ji)、陰(yin)(yin)極(ji)(ji)(ji)的(de)(de)極(ji)(ji)(ji)化(hua)(hua)(hua)并不總是(shi)同(tong)時以同(tong)種(zhong)程度發(fa)生,有些情(qing)(qing)況(kuang)下,陽(yang)極(ji)(ji)(ji)發(fa)生較大的(de)(de)極(ji)(ji)(ji)化(hua)(hua)(hua),而有些情(qing)(qing)況(kuang)下則(ze)是(shi)陰(yin)(yin)極(ji)(ji)(ji)發(fa)生較大的(de)(de)極(ji)(ji)(ji)化(hua)(hua)(hua)。在前一(yi)種(zhong)情(qing)(qing)況(kuang)下,反應(ying)由(you)陽(yang)極(ji)(ji)(ji)控(kong)制;后一(yi)種(zhong)情(qing)(qing)況(kuang)下,反應(ying)由(you)陰(yin)(yin)極(ji)(ji)(ji)來(lai)(lai)(lai)控(kong)制(圖1-1a和(he)圖1-1c)。為(wei)了提(ti)高金屬材(cai)料的(de)(de)耐腐(fu)蝕性(xing)(xing),可以通(tong)過(guo)提(ti)高其極(ji)(ji)(ji)化(hua)(hua)(hua)性(xing)(xing)能來(lai)(lai)(lai)實現(xian);作為(wei)能源的(de)(de)電(dian)池,則(ze)是(shi)通(tong)過(guo)降(jiang)(jiang)低其極(ji)(ji)(ji)化(hua)(hua)(hua)性(xing)(xing)能來(lai)(lai)(lai)實現(xian)的(de)(de)。
1. 鐵(tie) - 水(shui)體系的(de)極化
在鐵-水(shui)體系(xi)中,反應是(shi)(shi)受(shou)陰極(ji)(ji)控制(zhi)的,因為氫離子(zi)數量少,也(ye)就是(shi)(shi)說,陰極(ji)(ji)極(ji)(ji)化(hua)限制(zhi)著反應速(su)度;而氧氣(qi)(qi)是(shi)(shi)一種去極(ji)(ji)化(hua)劑,因為它(ta)增加了這個反應中的腐蝕(shi)電流及一定的腐蝕(shi)量。有一點應該考(kao)慮到,這就是(shi)(shi):極(ji)(ji)化(hua)可限制(zhi)腐蝕(shi)速(su)度,使(shi)之不(bu)能達(da)到最大值,如果(guo)不(bu)存(cun)在極(ji)(ji)化(hua),腐蝕(shi)速(su)度將可能達(da)到最大值。電解液(ye)(ye)中離子(zi)的緩(huan)慢(man)(man)移動、原(yuan)子(zi)緩(huan)慢(man)(man)地結合成氣(qi)(qi)體分子(zi)或電解液(ye)(ye)中離子(zi)的緩(huan)慢(man)(man)溶(rong)解,都可能是(shi)(shi)極(ji)(ji)化(hua)的表現形式。
2. 影響極化的因素
同其(qi)他的(de)(de)所有性(xing)(xing)能(neng)一樣,極(ji)(ji)(ji)(ji)(ji)化性(xing)(xing)能(neng)不僅因電(dian)極(ji)(ji)(ji)(ji)(ji)材料而(er)(er)異,而(er)(er)且與電(dian)解質有密切關系(xi),因此,極(ji)(ji)(ji)(ji)(ji)化的(de)(de)程度是不同的(de)(de)。一些(xie)腐(fu)蝕(shi)(shi)反應(ying)由于高自(zi)發性(xing)(xing)與低(di)極(ji)(ji)(ji)(ji)(ji)化性(xing)(xing),使得(de)腐(fu)蝕(shi)(shi)反應(ying)進行(xing)得(de)很(hen)快;而(er)(er)另一些(xie)腐(fu)蝕(shi)(shi)反應(ying),盡管(guan)它們有著明顯(xian)的(de)(de)腐(fu)蝕(shi)(shi)趨勢,但由于高極(ji)(ji)(ji)(ji)(ji)化性(xing)(xing)則使得(de)腐(fu)蝕(shi)(shi)反應(ying)進行(xing)得(de)非(fei)常慢。這(zhe)就是研究(jiu)、利用(yong)極(ji)(ji)(ji)(ji)(ji)化的(de)(de)目的(de)(de)所在。影響極(ji)(ji)(ji)(ji)(ji)化的(de)(de)因素(su)包括:
a. 增加反應(ying)面(mian)積,使(shi)腐蝕更容(rong)易發(fa)生,由(you)此(ci)而降低(di)了(le)極化率。
b. 攪拌或電(dian)解液流動(dong)帶走了(le)表(biao)面(mian)的腐蝕(shi)產物,從(cong)而提供了(le)大量與(yu)電(dian)極(ji)接觸的離子,增加(jia)了(le)腐蝕(shi)速(su)度(du)而降低了(le)極(ji)化;另一方面(mian),如果陰極(ji)反應起(qi)控制作用,則攪拌對腐蝕(shi)速(su)度(du)沒有影(ying)響。
c. 氧(yang)氣可(ke)有(you)效地使(shi)電(dian)極去極化(hua)或(huo)通(tong)過(guo)帶(dai)走反應產(chan)物原子態的氫使(shi)反應更快地進行。
d. 溫度增加,可使大(da)多數反應速度增加,因(yin)此降低了(le)極化率。
3. 極化圖
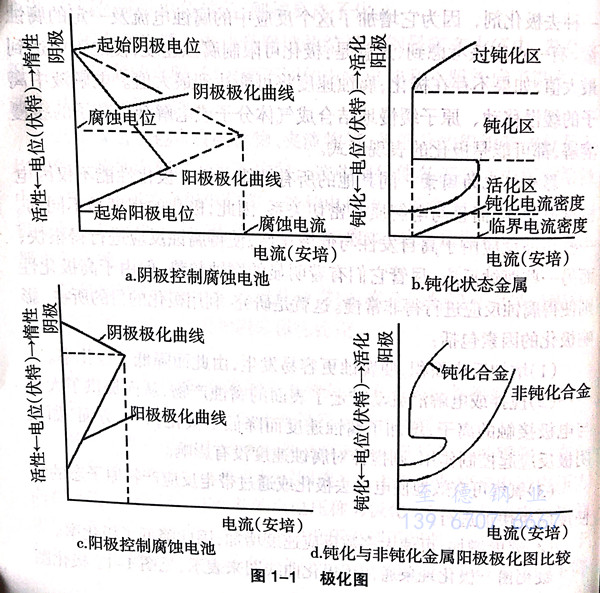
極(ji)(ji)化(hua)(hua)(hua)現象通常(chang)用極(ji)(ji)化(hua)(hua)(hua)曲(qu)(qu)線(xian)(xian)(xian)圖(tu)(tu)本(ben)示 ,見圖(tu)(tu)1-1。極(ji)(ji)化(hua)(hua)(hua)圖(tu)(tu)就是(shi)(shi)(shi)陽(yang)極(ji)(ji)電位和(he)陰(yin)極(ji)(ji)電位與其電流的(de)(de)關系圖(tu)(tu)。這些曲(qu)(qu)線(xian)(xian)(xian)也稱為Evans曲(qu)(qu)線(xian)(xian)(xian),這是(shi)(shi)(shi)以(yi)腐蝕科學的(de)(de)創始人之一 Ulick Evans命(ming)名的(de)(de)。圖(tu)(tu)1-1a表示由(you)陰(yin)極(ji)(ji)控制腐蝕電池(chi)(chi)的(de)(de)極(ji)(ji)化(hua)(hua)(hua)圖(tu)(tu)。圖(tu)(tu)1-1b為鈍化(hua)(hua)(hua)狀態由(you)金屬陽(yang)極(ji)(ji)控制腐蝕電池(chi)(chi)的(de)(de)極(ji)(ji)化(hua)(hua)(hua)曲(qu)(qu)線(xian)(xian)(xian)圖(tu)(tu),從圖(tu)(tu)1-1b可(ke)以(yi)看出,極(ji)(ji)化(hua)(hua)(hua)曲(qu)(qu)線(xian)(xian)(xian)并(bing)(bing)不是(shi)(shi)(shi)想象的(de)(de)那樣(yang)是(shi)(shi)(shi)沿直線(xian)(xian)(xian)極(ji)(ji)化(hua)(hua)(hua)的(de)(de),而是(shi)(shi)(shi)沿著“S”形(xing)曲(qu)(qu)線(xian)(xian)(xian)極(ji)(ji)化(hua)(hua)(hua)的(de)(de)。活化(hua)(hua)(hua)狀態-鈍化(hua)(hua)(hua)狀態轉變的(de)(de)電化(hua)(hua)(hua)學行為,可(ke)由(you)這些曲(qu)(qu)線(xian)(xian)(xian)加以(yi)說明。圖(tu)(tu)1-1c是(shi)(shi)(shi)由(you)陽(yang)極(ji)(ji)控制腐蝕電池(chi)(chi)的(de)(de)極(ji)(ji)化(hua)(hua)(hua)圖(tu)(tu),此圖(tu)(tu)可(ke)以(yi)說明氫氣對陰(yin)極(ji)(ji)極(ji)(ji)化(hua)(hua)(hua)的(de)(de)作用及聚(ju)集的(de)(de)金屬離(li)子和(he)腐蝕產物對陽(yang)極(ji)(ji)極(ji)(ji)化(hua)(hua)(hua)的(de)(de)作用。實際上,極(ji)(ji)化(hua)(hua)(hua)曲(qu)(qu)線(xian)(xian)(xian)并(bing)(bing)不是(shi)(shi)(shi)直線(xian)(xian)(xian),極(ji)(ji)化(hua)(hua)(hua)曲(qu)(qu)線(xian)(xian)(xian)的(de)(de)形(xing)狀取決于極(ji)(ji)化(hua)(hua)(hua)的(de)(de)具體(ti)過程。
4. 極化測定
耦合件極(ji)化的測(ce)(ce)定可以提供關于極(ji)化行(xing)為的精確信息,特別是對局部(bu)腐(fu)蝕的預測(ce)(ce)。用極(ji)化技術(shu)與(yu)臨界(jie)電位可以衡量金(jin)屬與(yu)合金(jin)在氯化物溶(rong)液(ye)中,點腐(fu)蝕與(yu)縫隙腐(fu)蝕的敏(min)感性(xing)。
5. 鈍(dun)化
有(you)(you)時(shi)材(cai)料(liao)發生腐(fu)蝕時(shi),會產(chan)生有(you)(you)黏附(fu)性的腐(fu)蝕產(chan)物(wu),這(zhe)種黏附(fu)性的腐(fu)蝕產(chan)物(wu)能夠起到保護材(cai)料(liao)免受進一步腐(fu)蝕作用(yong),這(zhe)也(ye)就是(shi)鈍化作用(yong)。這(zhe)些(xie)被鈍化的材(cai)料(liao)在特定的環境中腐(fu)蝕非常小,而(er)在其(qi)他(ta)環境中卻有(you)(you)可能產(chan)生相(xiang)當嚴重的腐(fu)蝕。例如,從電動序來看,鋁的腐(fu)蝕速度應該是(shi)較高的,然而(er)實(shi)際上(shang),鋁在除鹵化物(wu)外的多數介質(zhi)里具有(you)(you)較強(qiang)的耐腐(fu)蝕能力(li)。這(zhe)種現象稱為(wei)鈍化。鎳、鈦(tai)、鋯、鉻(ge)和不銹(xiu)鋼等材(cai)料(liao)都是(shi)因為(wei)可自(zi)鈍化而(er)具備了(le)耐腐(fu)蝕的能力(li)。
通(tong)過研究極(ji)化(hua)(hua)(hua)(hua)曲(qu)(qu)(qu)線(xian),也就(jiu)(jiu)是(shi)Evans曲(qu)(qu)(qu)線(xian),可以(yi)幫助更好(hao)地理(li)解(jie)合(he)金(jin)的(de)(de)(de)鈍(dun)(dun)化(hua)(hua)(hua)(hua)。圖(tu)1-1b中顯示的(de)(de)(de)鈍(dun)(dun)化(hua)(hua)(hua)(hua)合(he)金(jin)的(de)(de)(de)陽極(ji)極(ji)化(hua)(hua)(hua)(hua)曲(qu)(qu)(qu)線(xian)明(ming)顯不同于沒有(you)鈍(dun)(dun)化(hua)(hua)(hua)(hua)的(de)(de)(de)合(he)金(jin),圖(tu)1-1d是(shi)鈍(dun)(dun)化(hua)(hua)(hua)(hua)與沒有(you)鈍(dun)(dun)化(hua)(hua)(hua)(hua)材料的(de)(de)(de)極(ji)化(hua)(hua)(hua)(hua)曲(qu)(qu)(qu)線(xian)比較圖(tu)。鈍(dun)(dun)化(hua)(hua)(hua)(hua)明(ming)顯的(de)(de)(de)是(shi)陽極(ji)極(ji)化(hua)(hua)(hua)(hua)的(de)(de)(de)結果。在(zai)金(jin)屬(shu)(shu)與環(huan)境之(zhi)間(jian),由金(jin)屬(shu)(shu)氧(yang)(yang)(yang)化(hua)(hua)(hua)(hua)物(wu)或(huo)化(hua)(hua)(hua)(hua)學反應吸收的(de)(de)(de)氧(yang)(yang)(yang)氣形成一層牢固的(de)(de)(de)保護薄膜,可以(yi)防止金(jin)屬(shu)(shu)與電解(jie)液(ye)進一步接觸電解(jie)。在(zai)金(jin)屬(shu)(shu)為鐵(tie)的(de)(de)(de)情(qing)況下,當有(you)更多的(de)(de)(de)氧(yang)(yang)(yang)可以(yi)到達(da)陰極(ji)的(de)(de)(de)金(jin)屬(shu)(shu)表(biao)(biao)面進行反應時,就(jiu)(jiu)可以(yi)形成一層保護性的(de)(de)(de)鈍(dun)(dun)化(hua)(hua)(hua)(hua)膜,金(jin)屬(shu)(shu)表(biao)(biao)面因此達(da)到鈍(dun)(dun)化(hua)(hua)(hua)(hua)狀(zhuang)態,對避免加速腐蝕起到了非常重要(yao)的(de)(de)(de)作(zuo)用(yong)。在(zai)特定(ding)的(de)(de)(de)情(qing)況下,特定(ding)的(de)(de)(de)合(he)金(jin)能否鈍(dun)(dun)化(hua)(hua)(hua)(hua)取決于陽極(ji)和陰極(ji)極(ji)化(hua)(hua)(hua)(hua)效果。
鈍(dun)化(hua)(hua)(hua)狀(zhuang)態合(he)金被(bei)廣泛用做熱交(jiao)換器結構的(de)(de)耐(nai)腐蝕(shi)材料,鈍(dun)化(hua)(hua)(hua)狀(zhuang)態金屬的(de)(de)耐(nai)腐蝕(shi)性取(qu)決于鉻含(han)量、環境中的(de)(de)氯化(hua)(hua)(hua)物(wu)和氧(yang)含(han)量以及溫度。在特定的(de)(de)條件下達到鈍(dun)化(hua)(hua)(hua)狀(zhuang)態,取(qu)決于各種鈍(dun)化(hua)(hua)(hua)因(yin)素(su)的(de)(de)相對(dui)值能否超(chao)過其阻礙鈍(dun)化(hua)(hua)(hua)的(de)(de)因(yin)素(su)。例如(ru),高的(de)(de)鉻含(han)量有利(li)于鈍(dun)化(hua)(hua)(hua),低的(de)(de)溫度有利(li)于鈍(dun)化(hua)(hua)(hua),含(han)有去(qu)鈍(dun)化(hua)(hua)(hua)離子的(de)(de)氯化(hua)(hua)(hua)物(wu)阻礙鈍(dun)化(hua)(hua)(hua),而氧(yang)有利(li)于鈍(dun)化(hua)(hua)(hua)。
6. 鈍化狀態合金的行(xing)為
盡(jin)管鈍(dun)(dun)化(hua)狀態(tai)(tai)材(cai)(cai)料(liao)在特定的環境下,鈍(dun)(dun)化(hua)狀態(tai)(tai)材(cai)(cai)料(liao)腐(fu)(fu)蝕(shi)非常小,但在其他情況下可能(neng)腐(fu)(fu)蝕(shi)相當嚴重。相反(fan),通常顯示(shi)鈍(dun)(dun)化(hua)狀態(tai)(tai)的合金(jin)在非鈍(dun)(dun)化(hua)狀態(tai)(tai)下,常常是非常活潑的。某些元素可以(yi)擊穿(chuan)鈍(dun)(dun)化(hua)膜,造(zao)成(cheng)鈍(dun)(dun)化(hua)膜不連續處的金(jin)屬被腐(fu)(fu)蝕(shi)。例如(ru),氯離子(zi)破壞鋁、鐵以(yi)及(ji)不銹鋼的鈍(dun)(dun)化(hua),造(zao)成(cheng)點(dian)腐(fu)(fu)蝕(shi)。因此,使用(yong)鈍(dun)(dun)化(hua)狀態(tai)(tai)金(jin)屬的用(yong)戶應(ying)特別注(zhu)意(yi)點(dian)腐(fu)(fu)蝕(shi)、應(ying)力腐(fu)(fu)蝕(shi)開裂、敏化(hua)以(yi)及(ji)貧氧腐(fu)(fu)蝕(shi)等。
對(dui)于(yu)金屬的(de)耐腐蝕性,希望有(you)(you)較(jiao)高的(de)極化性能;對(dui)于(yu)作為能源的(de)電池或(huo)金屬的(de)表(biao)面處(chu)理(li),卻要求有(you)(you)較(jiao)低的(de)極化性能。同其(qi)他的(de)所有(you)(you)性能一樣,極化性能不僅(jin)因(yin)電極材料而異,也與電解質密切相(xiang)關。
二、不銹鋼的極化曲線
不銹鋼的極化曲線,見圖1-2。圖1-2描述了不銹鋼以及有活化、鈍化轉變的合金電極動力學過程,并按電位分為活化區(A)、鈍化區(P)和過鈍化區(T)。應用陽極極化曲線(εm)及相關的陰極極化曲線(圖1-2中的①、②、③、④),可以求得腐蝕電位和腐蝕電流密度(圖1-2中的陽極化曲線和陰極化曲線的交點A、B、C、D、E、F)。
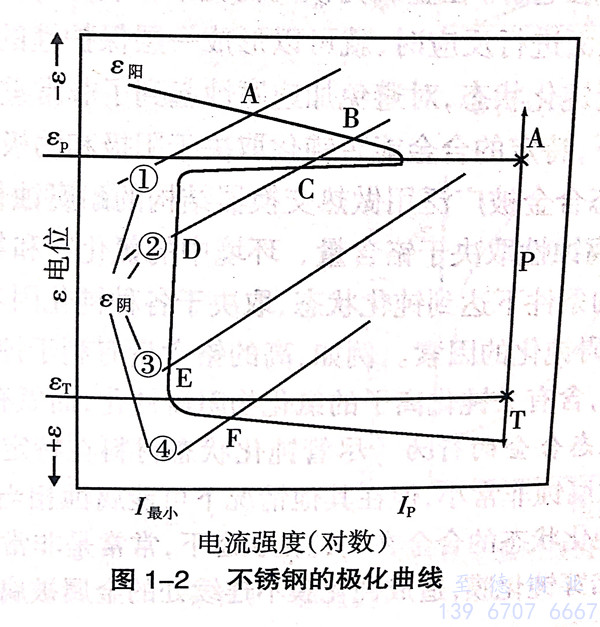
金(jin)屬或合金(jin)在(zai)不同條(tiao)件下(xia),其電(dian)(dian)化(hua)學腐蝕(shi)(shi)有四種狀(zhuang)態(tai)(tai)(tai):一是(shi)活化(hua)狀(zhuang)態(tai)(tai)(tai),腐蝕(shi)(shi)電(dian)(dian)流強(qiang)度較大,因(yin)而腐蝕(shi)(shi)速度較快;二是(shi)相對穩定狀(zhuang)態(tai)(tai)(tai),即(ji)金(jin)屬處于(yu)可以(yi)鈍(dun)(dun)化(hua)也可以(yi)活化(hua)狀(zhuang)態(tai)(tai)(tai);三是(shi)鈍(dun)(dun)化(hua)穩定狀(zhuang)態(tai)(tai)(tai),金(jin)屬只處于(yu)鈍(dun)(dun)化(hua)狀(zhuang)態(tai)(tai)(tai),而且是(shi)穩定的(de),能(neng)夠自動鈍(dun)(dun)化(hua),只有很(hen)小的(de)腐蝕(shi)(shi)電(dian)(dian)流,腐蝕(shi)(shi)速度很(hen)小;四是(shi)過鈍(dun)(dun)化(hua)狀(zhuang)態(tai)(tai)(tai),當金(jin)屬處于(yu)過鈍(dun)(dun)化(hua)狀(zhuang)態(tai)(tai)(tai)時(shi)有較高的(de)腐蝕(shi)(shi)電(dian)(dian)流。
為(wei)了(le)提高(gao)不銹鋼(gang)的耐腐蝕性(xing)能(neng),我們希望:
a. 不(bu)銹鋼易處(chu)于鈍化態,也就(jiu)是可以自動鈍化;
b. 不銹(xiu)鋼鈍化后腐蝕(shi)電流密度要(yao)很低(di);
c. 不銹鋼(gang)鈍(dun)化狀態的(腐蝕)電位(wei)范(fan)圍(wei)要(yao)寬。
上述三點(dian)分別(bie)指出了不銹鋼獲(huo)得鈍(dun)(dun)化的必要條件、鈍(dun)(dun)化狀(zhuang)態的腐(fu)蝕速度和鈍(dun)(dun)化狀(zhuang)態的相對穩定性。
不(bu)銹鋼只(zhi)有(you)處在(zai)鈍(dun)化(hua)(hua)狀態(tai)方能耐(nai)腐(fu)蝕(shi)(shi),這時鈍(dun)化(hua)(hua)狀態(tai)腐(fu)蝕(shi)(shi)電流最(zui)小,腐(fu)蝕(shi)(shi)速(su)度最(zui)慢,其他三種狀態(tai)下(xia)不(bu)銹鋼都(dou)是不(bu)耐(nai)腐(fu)蝕(shi)(shi)的(de)。由(you)此可見,不(bu)銹鋼的(de)“不(bu)銹”是相對的(de),只(zhi)是腐(fu)蝕(shi)(shi)速(su)度比較慢就是了。



